1. Gaya Van der Waals
Gaya Van der Waals merupakan salah satu jenis gaya tarik-menarik di antara molekul-molekul. Gaya ini timbul dari gaya London dan gaya antardipol-dipol. Jadi, gaya Van der Waals dapat terjadi pada molekul nonpolar maupun molekul polar.
Gaya ini diusulkan pertama kalinya oleh Johannes Van der Waals (1837–1923). Konsep gaya tarik antarmolekul ini digunakan untuk menurunkan persamaan-persamaannya tentang zat-zat yang berada dalam fase gas.
Kejadian ini disebabkan adanya gaya tarik-menarik antara inti atom dengan elektron atom lain yang disebut gaya tarik-menarik elektrostatis (gaya coulumb). Umumnya terdapat pada senyawa polar.
Untuk molekul nonpolar, gaya Van der Waals timbul karena adanya dipol-dipol sesaat atau gaya London.
Gaya Van der Waals ini bekerja bila jarak antarmolekul sudah sangat dekat, tetapi tidak melibatkan terjadinya pembentukan ikatan antaratom. Misalnya, pada suhu –160 °C molekul Cl2 akan mengkristal dalam lapisanlapisan tipis, dan gaya yang bekerja untuk menahan lapisan-lapisan tersebut adalah gaya Van der Waals.
Paling sedikit terdapat tiga gaya antarmolekul yang berperan dalam terjadinya gaya Van der Waals, yaitu gaya orientasi, gaya imbas, dan gaya dispersi.
a. Gaya orientasi
 Gaya orientasi terjadi pada molekul-molekul yang mempunyai dipol permanen atau molekul polar. Antaraksi antara kutub positif dari satu molekul dengan kutub negatif dari molekul yang lain akan menimbulkan gaya tarik-menarik yang relatif lemah. Gaya ini memberi sumbangan yang relatif kecil terhadap gaya Van der Waals, secara keseluruhan.
Gaya orientasi terjadi pada molekul-molekul yang mempunyai dipol permanen atau molekul polar. Antaraksi antara kutub positif dari satu molekul dengan kutub negatif dari molekul yang lain akan menimbulkan gaya tarik-menarik yang relatif lemah. Gaya ini memberi sumbangan yang relatif kecil terhadap gaya Van der Waals, secara keseluruhan.Kekuatan gaya orientasi ini akan semakin besar bila molekul-molekul tersebut mengalami penataan dengan ujung positif suatu molekul mengarah ke ujung negatif dari molekul yang lain. Misalnya, pada molekul-molekul HCl.
b. Gaya imbas
Gaya imbas terjadi bila terdapat molekul dengan dipol permanen, berinteraksi dengan molekul dengan dipol sesaat. Adanya molekul-molekul polar dengan dipol permanen akan menyebabkan imbasan dari kutub molekul polar kepada molekul nonpolar, sehingga elektron-elektron dari molekul nonpolar tersebut mengumpul pada salah satu sisi molekul (terdorongatau tertarik), yang menimbulkan terjadinya dipol sesaat pada molekul nonpolar tersebut.
Terjadinya dipol sesaat akan berakibat adanya gaya tarik-menarik antardipol tersebut yang menghasilkan gaya imbas. Gaya imbas juga memberikan andil yang kecil terhadap keseluruhan gaya Van der Waals.
2. Gaya london
Gaya london adalah gaya tarik-menarik yang sifatnya lemah antara atom atau molekul yang timbul dari pergerakan elektron yang acak di sekitar atom-atom. Karena elektron bergerak secara acak di sekitar inti atom, maka suatu saat terjadi ketidakseimbangan muatan di dalam atom. Akibatnya terbentuk dipol yang sesaat.
Dipol-dipol yang berlawanan ini saling berikatan, walau sifatnya lemah. Adanya gaya-gaya ini terutama terdapat pada molekul-molekul nonpolar yang dikemukakan pertama kalinya oleh Fritz London.
Perhatikan gambar
Setiap atom helium mempunyai sepasang elektron. Apabila pasangan elektron tersebut dalam peredarannya berada pada bagian kiri bola atom, maka bagian kiri atom tersebut menjadi lebih negatif terhadap bagian kanan yang lebih positif. Akan tetapi karena pasangan elektron selalu beredar maka dipol tadi tidak tetap, selalu berpindah-pindah (bersifat sesaat). Polarisasi pada satu molekul akan memengaruhi molekul tetangganya. Antara dipol-dipol sesaat tersebut terdapat suatu gaya tarik-menarik yang mempersatukan molekul-molekul nonpolar dalam zat cair atau zat padat.
3. Ikatan hidrogen
Ikatan hidrogen adalah gaya tarik-menarik yang cukup kuat antara molekul-molekul polar (mengandung atom-atom sangat elektronegatif, misalnya F, O, N) yang mempunyai atom hidrogen. Ikatan ini dilambangkan dengan titik-titik (...).
Contoh:
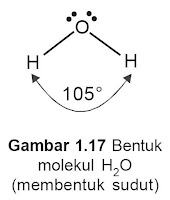
Ikatan hidrogen yang terjadi dalam molekul air. Di dalam molekul air, atom O bersifat sangat elektronegatif sehingga pasangan elektron antara atom O dan H lebih tertarik ke arah atom O. Dengan demikian terbentuk suatu dipol.
Gaya tarik-menarik antardipol ini yang melalui atom hidrogen disebut ikatan hidrogen.
Senyawa yang di dalamnya terdapat ikatan hidrogen umumnya memiliki titik didih yang tinggi. Sebab untuk memutuskan ikatan hidrogen yang terbentuk diperlukan energi lebih besar dibandingkan senyawa yang sejenis, tetapi tanpa adanya ikatan hidrogen.
H2O dengan struktur H–O–H dan senyawa yang mempunyai gugus O–H seperti alkohol (R–OH) terutama yang jumlah atom C-nya kecil, senyawa tersebut akan bersifat polar dan mempunyai ikatan hidrogen.
Begitu juga NH3 dengan struktur:
atau senyawa amina (R–NH2), mempunyai ikatan hidrogen.
Pada molekul H–F, ujung molekul H lebih bermuatan positif dan ujung molekul F lebih bermuatan negatif. Dari ujung yang berbeda muatan tersebut (dipol) mengadakan suatu ikatan dan dikenal dengan ikatan hidrogen.
Pada molekul HF, ikatan antara atom H dan F termasuk ikatan kovalen. Sedangkan ikatan antarmolekul HF (molekul HF yang satu dengan molekul HF yang lainnya) termasuk ikatan hidrogen.
Pengaruh Ikatan Hidrogen pada Titik Didih
Titik didih suatu zat dipengaruhi oleh:
a. Mr, jika Mr besar maka titik didih besar dan Mr kecil maka titik didih kecil.
b. Ikatan antarmolekul, jika ikatan kuat maka titik didih besar dan ikatan lemah maka titik didih kecil.
Perhatikan data Mr dan perbedaan keelektronegatifan senyawa golongan halogen (VIIIA) berikut.
Titik cair dan titik didih senyawa-senyawa yang mempunyai persamaan dalam bentuk dan polaritas, naik menurut kenaikkan massa molekul. Perhatikan titik didih hidrida unsur-unsur golongan IVA pada gambar di samping. Dari CH4 sampai SnH4, titik didih naik secara beraturan.
Untuk hidrida unsur-unsur golongan VIA (H2O, H2S, H2Se, dan H2Te) terdapat penyimpangan yang sangat mencolok pada H2O. Penyimpangan yang sama juga terdapat pada NH3 dengan hidrida unsur-unsur golongan VA lain (PH3, AsH3, dan SbH3) dan juga pada HF dengan hidrida unsur-unsur golongan VIIA lainnya (HCl, HBr, HI, dan HAt). Sifat yang abnormal dari HF, H2O, dan NH3 tersebut dijelaskan dengan konsep ikatan hidrogen.
Seperti kita ketahui, F, O, dan N adalah unsur-unsur yang sangat elektronegatif. Oleh karena itu, ikatan F–H, O–H, dan N–H adalah ikatan-ikatan yang sangat polar. Dalam HF, H2O, NH3, dan senyawa-senyawa lain yang mengandung ikatan F–H, O–H, atau N–H, atom H sangat positif. Dalam senyawa-senyawa seperti itu terdapat suatu ikatan, yang disebut ikatan hidrogen, yaitu ikatan karena gaya tarik-menarik elektrostatik antara atom hidrogen yang terikat pada atom berkeelektronegatifan besar (atom F, O, atau N) dengan atom berkeelektronegatifan besar dari molekul tetangga, baik antarmolekul sejenis maupun yang berlainan jenis.
sumber : bse kimia